DOCUMENTS DE BASE
La radioactivité
est le plus souvent abordée sous l'angle de ses risques. Elle l'est
plus rarement sous l'angle de ses nombreuses applications, et presque jamais
(hors des publications spécialisées) sous l'angle du phénomène
physique lui-même. Quant à sa riche histoire, elle est parfois
réduite à ses aspects anecdotiques (ah, le « hangar
» des Curie !). Il a donc paru utile de rassembler un dossier en
3 parties qui traitent du phénomène physique de la radioactivité,
de l'histoire de la compréhension de ce phénomène
et de sa perception par la société, et enfin de ses multiples
applications contemporaines.
 Le phénomène physique
|
Par exemple, du potassium se transforme en
calcium en émettant un électron (et un antineutrino). On
parle souvent de désintégration, mais le mot est trompeur
car le noyau est plus solidement lié après la transmutation
qu'avant.
La radioactivité serait resté une simple curiosité de laboratoire si les particules émises au cours de ce phénomène ne possédaient pas une énergie considérable: cette énergie peut être maîtrisée, mais elle peut également provoquer des ravages. Elle est présente depuis des milliards d'années autour de nous: la radioactivité vient pour 2/3 du sol et de l'air ambiant et pour 1/3 des utilisations médicales en imagerie et en radiothérapie. La radioactivité est une conséquence de réarrangements dans les noyaux. Ceux-ci sont formés de protons et de neutrons, mais il n'est pas possible d'associer n'importe quel nombre de protons et de neutrons pour former un noyau. À la différence des molécules qui peuvent rassembler un nombre immense d'atomes (pensons aux polymères ou aux macromolécules) il n'existe qu'un nombre restreint de noyaux possibles, quelques milliers tout au plus, et la plupart sont instables. Tout est une question d'énergie et nous allons consacrer un peu de temps à comprendre comment se répartit cette énergie, avant de passer aux différentes formes de transmutations et à leurs effets dans la matière et dans les corps vivants. retour au sommaire |
La matière est constituée
d'atomes, le plus souvent assemblés en molécules ou en cristaux.
Ces atomes sont très petits, de l'ordre du dix milliardième
de mètre, et ils sont très nombreux : 6x1023 atomes
par gramme d'hydrogène par exemple. Ils sont eux-mêmes formés
d'un nuage d'électrons au sein duquel est enfoui un noyau cent mille
fois plus petit: si le nuage électronique avait la taille de
la place de la Concorde, le noyau aurait la taille d'un petit pois.

La place de la Concorde La taille du noyau est donc de l'ordre du femtomètre
(un millionième de milliardième de mètre) que les
physiciens ont rebaptisé fermi (fm) en l'honneur d'Enrico Fermi.
À cette échelle, les énergies se mesurent en MeV (millions
d'électron-volts), unité mieux adaptée que le joule.
1 MeV ne représente que 160 millionièmes de milliardièmes
de joule, mais les atomes (et donc leurs noyaux) sont nombreux: si tous
les noyaux d'un gramme d'hydrogène possèdent chacun une énergie
de 1 MeV, ce gramme possède une énergie de 100 milliards
de joules, soit 30 MWh, l'énergie de 2 tonnes de pétrole
ou de 25 tonnes de TNT. On voit ainsi apparaître l'immense quantité
d'énergie stockée dans les noyaux.
|
Formant les noyaux, protons et neutrons sont
appelés des nucléons, et le nombre total A = Z+N de
nucléons est le nombre de masse du noyau. On parle alors de carbone
12 (Z=6, N=6) noté 12C, de carbone 14 (Z=6, N=8) noté
14C
ou d'uranium 238 (Z=92, N=146) noté 238U. On donne le
nom d'isobares aux noyaux de même nombre de masse mais de numéro
atomique différent comme l'argon 40, le potassium 40 et le calcium
40.
Les protons du noyau ayant tous la même charge électrique se repoussent, il doit donc y avoir une «colle» pour assurer la cohésion des noyaux. Avec beaucoup d'imagination, on l'a appelée la force nucléaire forte (ou interaction forte). Elle possède des caractéristiques étonnantes, outre son intensité : sa portée se limite à quelques fermis, elle est attractive au-delà de 1 fm, mais répulsive en deçà. 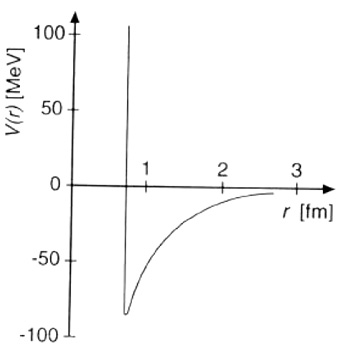
Représentation (très schématique) de la forme du potentiel nucléaire: répulsion intense à très courte distance, puis attraction diminuant exponentiellement avec la distance. Les nucléons se collent ainsi les uns aux autres mais en gardant leurs distances: il y a saturation de la force nucléaire. Le volume du noyau est ainsi proportionnel au nombre de nucléons, et son rayon est voisin de 1.2 A1/3 fm: les noyaux ont tous des tailles comparables (4 fm pour le calcium, 7 fm pour le plomb). Leur bord est cependant diffus et ils ressemblent plus des sacs où se promènent des boules de coton qu'à un empilement de boules de billard. 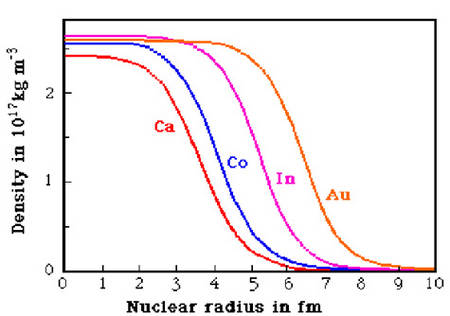
Rayons de quelques noyaux La «colle» nucléaire assure la cohésion du noyau, ce qui signifie qu'il faut faire un effort pour séparer les nucléons et donc apporter de l'énergie au noyau. Inversement de l'énergie est libérée quand les nucléons se collent les uns aux autres. Cette énergie est l'énergie de liaison. La relation d'Einstein E=mc2 implique que la masse du noyau est inférieure, de 1% environ, à la somme des masses de ses nucléons: ce défaut de masse a été mesuré pour les noyaux les plus stables par Francis Aston à partir de 1920. retour au sommaire |
| Puisque de l'énergie
est libérée par l'assemblage des nucléons, pourquoi
tous les nucléons de l'univers ne se rassemblent-ils pas en un noyau
gigantesque? Pour le comprendre, et pour comprendre ce qui se
passe dans un noyau, Aston a tracé la courbe mesurant l'énergie
de liaison des noyaux en fonction de leur (nombre de) masse A, ou plus
exactement l'énergie de liaison par nucléon E/A.
Cette courbe est très riche d'enseignements:
qu'y voit-on en effet? D'abord E/A est à peu près constante,
de l'ordre de 8 MeV pour la plupart des noyaux. C'est trop peu pour augmenter
le nombre total de nucléons (il faut 940 MeV pour créer un
nucléon), mais assez pour transformer un proton en neutron, et inversement.
Ensuite on note que E/A augmente jusqu'à A ~ 50 (la position du
fer et du nickel) avant de diminuer ensuite peu à peu. Enfin on
remarque quelques à-coups, certains noyaux apparaissant plus liés
que la « normale », en particulier l'hélium et certains
noyaux ayant à la fois un nombre pair de protons et un nombre pair
de neutrons comme le carbone 12 ou l'oxygène 16.
Mais bien sûr, les nucléons sont
moins liés quand ils sont proches de la surface que lorsqu'ils sont
enfouis à l'intérieur, puisqu'ils ont moins de voisins. L'énergie
de liaison par nucléon est diminuée d'un terme –aSA2/3,
proportionnel à la surface. Le coefficient aS est aussi de l'ordre
de 15 MeV, l'effet est donc important pour les petits noyaux.
|
Une troisième complication vient
de la charge électrique des protons: leur répulsion électrique
induit une pénalité coulombienne –aCZ2/A1/3
proportionnelle au carré de la charge électrique Z. Le coefficient
aC ~ 0.6 MeV semble petit, mais il finit par dominer pour Z>50.
Il est possible d'alléger cette pénalité en augmentant
le nombre de neutrons, qui apportent plus de colle sans créer de
répulsion. Mais ce n'est qu'un palliatif temporaire puisque
l'attraction est proportionnelle au nombre A de nucléons alors que
la répulsion augmente comme le carré de la charge Z et finit
par l'emporter.
Il y a une quatrième complication, d'origine quantique elle aussi: protons (et neutrons) minimisent leur énergie en s'appariant (par paires de spins inverses) et les noyaux pairs-pairs sont donc plus stables que les pairs-impairs et que les impairs-impairs. Cela se paramétrise par un bonus ou une pénalité d'appariement ±ð(A,Z). On a remarqué également que les noyaux étaient particulièrement stables quand ils possédaient certains nombres, dits « magiques », de protons ou de neutrons: 8, 20, 28, 50, 82, 126, 184,nombres dont l'origine est à peu près, mais pas complètement, comprise. En recollant les morceaux, nous avons l'équation de Bethe et Weizsäcker pour l'énergie de liaison par nucléon : E/A = aV –aSA2/3 –aA(N-Z)2/A –aCZ2/A /3 ±ð(A,Z). Mais nous avons maintenant bien plus qu'une explication de la courbe E(A) d'Aston, nous avons une estimation de l'énergie de liaison de n'importe quel noyau, quelle que soit son nombre Z de protons et N de neutrons. Nous pouvons alors tracer la carte des noyaux possibles en portant cette énergie de liaison en fonction de Z et de N. Cela nous donne une sorte de paysage dont le relief représente cette énergie de liaison, les creux correspondant aux noyaux les plus liés, les pics aux noyaux les moins liés. Minimiser l'énergie correspond à rechercher les creux les plus profonds de ce paysage. Nous avons déjà remarqué qu'il ne peut pas y avoir d'excès considérable de protons ou de neutrons, et qu'il ne peut pas non plus y avoir de noyau très lourd en raison de la répulsion électrique. Les 3.000 à 5.000 noyaux possibles s'alignent donc le long d'une courbe qui suit N=Z au début avant de s'infléchir peu à peu. La formule de Bethe et Weizsäcker indique ensuite que l'énergie de liaison, pour un nombre de masse A donné, est quadratique en Z : cela implique que cette énergie est minimale pour une valeur précise de Z et qu'elle augmente si Z s'écarte, en plus ou un moins, de chaque côté. Dans notre paysage, nous avons donc une vallée parabolique dont le fond suit la valeur optimale de Z pour A (et donc N=A-Z) donné. On l'appelle la vallée de stabilité.
Mais non seulement le nombre de noyaux possibles est limité, la plupart d'entre eux disparaissent en quelques secondes: ils sont instables, radioactifs. Mais pourquoi?
retour au sommaire |
| C'est un principe général
de physique que tout système tend à minimiser son énergie.
A priori, il n'est donc pas très surprenant de voir la transmutation
d'un noyau en un autre si cela conduit à minimiser l'énergie
totale. Mais alors pourquoi ne sont-ils pas tous radioactifs, pourquoi
l'univers n'est-il pas seulement composé de fer? Parce qu'il ne
suffit pas que les niveaux d'énergie soient dans le bon sens pour
permettre une transition spontanée, encore faut-il qu'il n'y ait
pas de barrière infranchissable entre les deux niveaux, et que le
temps nécessaire à la transition ne soit pas trop long !
Prenons par exemple un noyau lourd comme l'uranium 238 (Z=92). La courbe d'Aston indique que l'énergie de liaison par nucléon diminue au delà du fer, essentiellement en raison de la répulsion électrostatique grandissante. Il devient donc peu à peu énergétiquement favorable d'avoir deux noyaux au lieu d'un, par exemple un noyau de baryum (Z=56) et un de krypton (Z=36). C'est une fission spontanée du noyau. Mais cela exige que le noyau plus ou moins sphérique d'uranium (forme qui assure qu'un maximum de nucléons soit à l'intérieur plutôt qu'en surface) se déforme d'abord en une sorte de haltère avant de se scinder en deux.
Mais la surface augmente alors fortement,
ce qui implique que l'énergie est plus grande dans l'étape
intermédiaire. Autrement dit, il y a une barrière énergétique
qui s'oppose à cette fission spontanée, barrière que
l'on peut franchir en apportant de l'énergie au noyau initial, par
exemple en le bombardant de neutrons. Cette fission induite est utilisée
dans les réacteurs nucléaires (l'énergie libérée
par la fission est supérieure à celle des neutrons).
Il est rare qu'un noyau lourd se scinde spontanément
en deux noyaux de taille comparable, il est bien plus « intéressant
» d'exploiter la cohésion très forte du noyau d'hélium
(souvenons-nous du pic sur la courbe d'Aston) en scindant le noyau lourd
en un noyau juste un peu plus léger et un noyau d'hélium.
La barrière est moins infranchissable et donc le processus plus
probable.
Cette carte des modes de transmutation des
noyaux indique en vert clair les noyaux susceptibles de fission spontanée
et en jaune ceux qui émettent plutôt des alphas (les deux
modes peuvent bien sûr être simultanément possibles,
comme pour l'uranium 238). Ces deux modes ne concernent que les noyaux
les plus lourds, la plupart des autres transmutations impliquent des transitions
bêta (vocable aussi dû à Rutherford). De quoi s'agit-il?
|
Le mécanisme est similaire à
celui de l'émission de photons par les atomes, à ceci près
que le photon a beaucoup plus d'énergie et donc une longueur d'onde
beaucoup plus courte que la lumière visible ou les rayons X : ce
sont les rayons gammas. Le noyau peut d'ailleurs émettre plusieurs
photons gammas en cascade dans ce processus de désexcitation.
Par exemple, le cobalt 60 se transmute par ß- en nickel 60 excité,
qui se désexcite immédiatement en émettant en cascade
deux photons gamma de 1.17 MeV et 1.33 MeV. Sauf cas très exceptionnels,
la transition gamma est beaucoup plus rapide que les transitions alpha
ou bêta, et est instantanée à l'échelle humaine.
Le noyau résultant d'une transmutation peut fort bien être radioactif lui aussi. Il se constitue ainsi des chaînes radioactives, des suites de noyaux se transmutant en cascade. À un instant donné, le noyau «père» coexiste avec toute la chaîne de ses descendants (équilibre radioactif). Les plus connues sont les chaînes de désintégration alpha des noyaux lourds, par exemple celle qui conduit de l'uranium 238 au plomb 206, en passant par le radium 226, le radon 222, ou le polonium 210.
Chaque désintégration alpha diminue
de 2 le nombre de protons et de 2 le nombre de neutrons. Les noyaux successifs
deviennent de plus en plus excédentaires en protons, et l'équilibre
se rétablit en entrecoupant les transitions alpha par des transitions
ß+.
Le tableau suivant donne quelques périodes de noyaux d'usage courant. Remarquons l'énorme éventail de périodes (de la picoseconde à plusieurs milliards d'années), et notons que l'éventail est aussi large pour les transitions alpha que pour les transitions bêta.
Il y a bien évidemment une corrélation
inverse entre période et activité: un gramme d'une substance
de nombre de masse A et de période t1/2 a une activité de
1.3x1016x(1 an/t1/2)/A becquerels. Cela semble colossal, parce que le becquerel
est une unité minuscule. Si la radioactivité d'un gramme
de radium est de 37 milliards de becquerels (c'était l'ancienne
unité d'activité, la curie), celle d'un gramme d'uranium
n'est de 12.000 becquerels. Les objets courants de notre environnement
sont toujours un peu radioactifs : 13 Bq pour un litre d'eau de mer, 1.000
Bq pour un kg de granit, 7.000 Bq pour un corps humain (4.500 dus au potassium
40, 2.500 dus au carbone 14). Ces radioactivités, aussi faibles
soient-elles, sont facilement détectables et mesurables.
retour au sommaire |
| La question de l'origine des noyaux
s'écarte un peu de la radioactivité au sens strict,
mais elle permet de mieux comprendre les relations entre les divers noyaux.
La courbe d'Aston montre que les éléments plus légers
que le fer sont moins liés que ce dernier, et qu'il en est
de même des éléments situés au delà de
lui. En d'autres termes, de l'énergie est libérée
en assemblant des éléments légers, en les fusionnant,
et de l'énergie est libérée en dissociant des éléments
lourds, en les fissionnant.
Fusionner des noyaux n'est pas si simple : avant que la force nucléaire ne colle ensemble tous les nucléons (en libérant l'énergie de liaison correspondante), il faut que les noyaux s'approchent à quelques fermis l'un de l'autre. Mais les noyaux possèdent tous des charges électriques positives et se repoussent violemment au delà de ces quelques fermis. Il est indispensable qu'ils soient projetés violemment les uns contre les autres pour vaincre cette répulsion, et donc qu'ils possèdent une grande énergie cinétique. Sauf à disposer d'un accélérateur, la seule possibilité est que le milieu soit très chaud, à des températures dépassant 10 millions de degrés comme on n'en trouve qu'au cœur des étoiles, et pendant les premières minutes du big bang. C'est pourquoi on parle de fusion thermonucléaire. Si l'on considère maintenant l'abondance dans l'univers des différents noyaux, on constate que le noyau le plus léger l'hydrogène, est de très loin le plus abondant et représente 90% des noyaux. Il est suivi d'assez loin par le second plus léger, l'hélium qui en représente 9%. Tous les autres arrivent à peine à 1% du total, d'où l'échelle logarithmique utilisée sur le graphique qui montre une décroissante régulière avec la masse. A quelques zig-zags près, dont les pics correspondent au carbone, à l'oxygène… et au fer, 100 fois plus abondant qu'il ne « devrait ». Tous ces pics correspondent aux noyaux particulièrement stables, leur présente n'est donc pas si étonnante et montre un lien entre énergie de liaison et abondance des noyaux.
Gamow a réalisé dès 1940
que l'on devait précisément s'attendre à pareille
distribution si les noyaux les plus légers s'agglutinent les uns
aux autres pour former successivement des noyaux de plus en plus lourds
au cours d'un processus dynamique encore à l'œuvre. Dans le cadre
de la théorie cosmologique du big bang, l'univers a traversé
une période si chaude dans le passé qu'aucun noyau n'aurait
pu y résister : à la sortie de cette phase, l'univers n'était
formé que de protons et de neutrons libres. Le calcul indique qu'il
devait y avoir 6 protons pour chaque neutron (en raison de la masse plus
légère du proton). Associer chaque paire de neutrons avec
une paire de protons pour former un noyau d'hélium conduit à
laisser 10 protons seuls pour chaque noyau d'hélium formé.
On retrouve bien les abondances relatives de l'hydrogène et de l'hélium.
Un mécanisme analogue est d'ailleurs à l'œuvre dans le Soleil
où 4 protons fusionnent en un noyau d'hélium (plus 2 positrons
et deux neutrinos), en libérant l'énergie qui permet au Soleil
de briller.
Mais cela n'explique pas l'origine des éléments plus lourds que le fer, dont la formation nécessite un apport d'énergie. Dans des étoiles très lourdes et très chaudes, une partie de l'énergie produite par les fusions peut être employée à cette fin. En présence d'un flux intense de neutrons, les noyaux peuvent en capturer et progresser ainsi en remontant la vallée de stabilité. |
Mais à capturer des neutrons, le noyau
devient de plus en plus instable, et il retrouve une meilleure stabilité
par une transition bêta moins. Si le noyau se transmute avant de
capturer un autre neutron, la synthèse suit à peu près
le fond de la vallée de stabilité jusqu'au bismuth 209. Il
faut pour cela un environnement stable, comme dans les étoiles géantes
rouges pendant le flash de l'hélium. On parle alors de processus
s (pour slow, lent). Le noyau peut au contraire capturer un autre neutron
avant de subir une transition bêta, et la synthèse ne suit
plus le fond de la vallée. Ce processus r (pour rapid) est uniquement
possible au cours d'une phase explosive, dans les supernovae.
Un processus similaire, le processus rp agit de l'autre côté de la vallée, dans les environnements très chauds et riches en protons (comme les novae, ou les bouffées X). Les noyaux s'enrichissent ainsi en protons. Enfin, les rayons cosmiques fabriquent également des noyaux, mais plutôt en brisant des noyaux plus lourds (processus de spallation). Tout ceci peut se résumer dans ce tableau périodique des éléments, où la couleur correspond au mécanisme principal de formation: 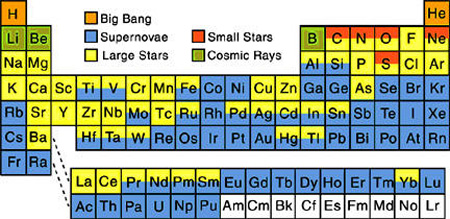 Avant de clore ce chapitre, disons un mot de la fission. En effet, les noyaux lourds une fois formés peuvent encore évoluer en se brisant en deux plus légers. La fission spontanée est rare, mais la fission provoquée par la collision d'un projectile (le plus souvent un neutron) sur une cible, un noyau lourd, est bien plus facile en comparaison. De plus, la fragmentation produit en général des neutrons secondaires : une réaction en chaîne est alors possible si ces neutrons vont percuter d'autres noyaux lourds, qui fissionnent à leur tour en produisant à nouveau d'autres neutrons qui à leur tour… ême si cela peut arriver spontanément
comme à Oklo, au Niger, où un réacteur naturel a fonctionné
pendant 400.000 ans dans un gisement d'uranium, il y a deux milliards d'années,
il n'est pas si simple de provoquer une réaction en chaîne.
En effet, les neutrons doivent trouver une cible minuscule, les noyaux,
qui ne mesurent que 7 fermis et se trouvent à 350.000 fermis les
uns des autres. Si la quantité de matériau fissile est trop
faible, les neutrons s'en échappent avant de provoquer une nouvelle
fission. Pour entretenir une réaction en chaîne, il est donc
indispensable d'en rassembler une quantité minimale, la masse critique,
de l'ordre de 50 kg pour l'uranium 235, ou 10 kg pour le plutonium 239.
C'est pour cela qu'on ne peut pas construire de tout petits réacteurs
nucléaires.
retour au sommaire |
| Revenons à la radioactivité
proprement dite, et à ses effets dans la matière.
Lors d'une transmutation, les particules émises par les noyaux radioactifs possèdent des énergies de l'ordre du MeV, très supérieures par conséquent aux énergies (chimiques) des liaisons atomiques et moléculaires des milieux traversés qui sont plutôt de l'ordre de l'électron-volt (eV), un million de fois plus faibles. Même en n'y déposant qu'une fraction de leur énergie, ces particules perturbent considérablement les milieux traversés : rupture de liaisons moléculaires, création de radicaux libres, amorçage de réactions chimiques ou physiques (comme l'apparition de bulles dans les liquides), créations de défauts dans les cristaux, et bien sûr chaleur (ce qui est exploité dans les centrales nucléaires). Les dégâts dépendent de la nature du projectile, de son énergie, et du milieu traversé (gaz, cristal, cellule vivante). Les particules électriquement chargées comme les alpha et les bêta arrachent des électrons aux atomes (qui deviennent des ions) qu'elles rencontrent le long de leur trajet. Elles perdent ainsi progressivement leur énergie et ralentissent. C'est en fin de parcours, quand la particule a beaucoup ralenti, que l'ionisation est la plus importante: en effet une particule lente passe plus de temps dans un atome et a plus de chances d'interagir avec lui. Les particules alpha sont beaucoup plus lourdes que les électrons et sont peu déviées : elles ont tout de l'éléphant dans un magasin de porcelaine. Elles perdent très rapidement leur énergie et sont donc vite immobilisées (une feuille de carton arrête une particule alpha de quelques MeV). Elles agissent donc pratiquement par contact : les alphas du radium ont brûlé la peau des doigts des Curie. La situation est similaire pour d'autres particules chargées et lourdes comme les protons ou les ions de carbone (utilisés en protonthérapie) qui interagissent d'autant plus fortement qu'elles sont ralenties : l'ionisation augmente fortement juste avant l'arrêt, c'est le pic de Bragg.
Les électrons (particules bêta), plus légers, perdent
moins d'énergie en interagissant avec les électrons atomiques
ou les noyaux, mais sont plus fortement déviés à chaque
fois : leur parcours est donc plus long et plus sinueux, évoquant
plus le chat que l'éléphant dans le magasin de porcelaine.
Leur pénétration est plus profonde avec un dépôt
d'énergie plus progressif que les alphas. Pour arrêter des
électrons de quelques MeV, il faut donc une épaisseur de
blindage plus importante : plusieurs mètres d'air, plusieurs centimètres
de tissu vivant, ou plusieurs millimètres d'aluminium. Les positrons
(bêta plus) interagissent comme des électrons, à ceci
près qu'ils finissent par s'annihiler avec un électron atomique
en donnant 2 gammas de 0.511 MeV chacun. Cette signature caractéristique
est utilisée dans la tomographie par émission de positrons
(ou TEP).
|
Les photons gamma peuvent entrer en collision
avec un électron atomique et lui communiquer une part importante
de leur énergie : c'est la diffusion Compton. L'électron
diffusé ionise ensuite son environnement. Le gamma interagit rarement,
d'où une moins grande nocivité que les alphas et bêtas,
et une pénétration profonde. Pour augmenter la probabilité
d'interaction, il vaut mieux employer des matériaux denses (ayant
beaucoup d'électrons dans un volume donné) comme le plomb
: pour arrêter 99.9% des gammas de 1 MeV, il faut 10 cm de plomb,
60 cm de béton ou un mètre de terre.
Les neutrons n'interagissent qu'avec un noyau,
et celui-ci occupe un très petit volume dans l'atome : les collisions
sont donc rares, et un flux de neutrons est donc extrêmement pénétrant.
Le neutron perd plus facilement son énergie (et est donc arrêté)
quand il entre en collision avec une cible de masse comparable à
la sienne. Un blindage contre les neutrons emploie donc un matériau
riche en noyaux légers comme l'eau, le graphite ou la paraffine.
Lors d'une collision, le neutron rebondit en général, mais
il peut être capturé par un noyau. Le noyau ainsi formé
a toutes chances d'être instable (en capturant un neutron, l'uranium
238 devient de l'uranium 239 dont la période n'est que de 23 mn).
C'est pour cela que les matériaux irradiés dans une centrale
deviennent radioactifs. Et nous avons vu que le choc d'un neutron brise
parfois le noyau (fission nucléaire).
retour au sommaire |
| Les effets des rayonnements
ionisants sur le vivant ont été très vite connus:
les rayons X endommageaient la peau des premiers radiologues, et le radium
a été très vite utilisé pour soigner des cancers.
Les effets se révèlent très variables selon le type
de rayonnement, selon les cellules touchées, selon la dose reçue
et selon la durée pendant laquelle a été reçue
cette dose. Ce n'est pas très surprenant puisque la même énergie
est répartie sur quelques cellules pour les alphas, quelques milliers
de cellules pour les bêtas et plus encore pour les gammas.
Les rayonnements ionisants modifient les molécules essentielles au fonctionnement cellulaire en brisant des liaisons chimiques. Ils peuvent créer des radicaux libres, dont la réactivité chimique est très forte et qui sont capables d'oxyder des protéines, ou les lipides des membranes cellulaires. Ils peuvent aussi briser l'un des brins de la double hélice de l'ADN, voire les deux, ou les liaisons entre les deux brins. Tous ces effets sont semblables à ceux d'autres « agressions » des cellules comme une élévation de température, une déshydratation, la présence de substances toxiques, ou l'activité des radicaux libres dus à la respiration cellulaire. Ces agressions sont très fréquentes (on estime que l'ADN subit constamment un millier de lésions par heure et par cellule) et elles sont sans doute à l'origine du vieillissement cellulaire. Les cellules disposent fort heureusement de mécanismes de réparation très efficaces. Ainsi, lorsqu'un seul brin de l'ADN est brisé, la réparation prend le brin intact comme modèle. Lorsque les deux brins sont brisés, la recopie n'est plus possible, et la cellule déclenche une sorte de « suicide cellulaire » appelé apoptose.
La réparation cellulaire parvient à
compenser les effets d'une faible dose de radiation, surtout si elle est
étalée dans le temps, mais elle est saturée en cas
de dose importante délivrée pendant un court laps de temps.
Les cellules qui ne parviennent pas à être réparées
meurent et les tissus se nécrosent. Si la nécrose n'est pas
trop étendue, l'organisme parvient à l'éliminer, et
à
remplacer les cellules mortes, sinon une lésion inflammatoire apparaît,
comme lors d'une brûlure, et des pathologies apparaissent.
|
L'existence de pathologies non cancéreuses
induites par les rayonnements a aussi été repérée
au travers d'études statistiques: les survivants d'Hiroshima ont
en effet montré des pathologies cardiaques, respiratoires ou digestives
un peu plus fréquentes que dans des populations équivalentes.
Ces pathologies sont probablement dues à un vieillissement cellulaire
induit par l'irradiation brutale reçue lors de l'explosion.
Il est clair que l'utilisation des grays n'est pas bien adaptée à l'évaluation des effets biologiques, et des risques encourus par une irradiation. La Commission internationale de protection radiologique (CIPR en anglais) a donc proposé de pondérer la dose reçue (mesurée en grays) par des coefficients qui tiennent compte de la nature du rayonnement et de la cible touchée. C'est ainsi qu'a été défini le sievert (Sv), ainsi nommé en l'honneur de Rolf Sievert, pionnier de la radioprotection: la dose reçue, mesurée en grays, est multipliée par un coefficient de pondération Q propre à chaque rayonnement et par un coefficient de pondération N propre à chaque organe humain. Ces coefficients de pondération sont empiriques, ils ont été estimés par la fréquence des cancers des survivants d'Hiroshima, et ils évoluent au fil des recherches. Le sievert a remplacé le rem qui vaut 0.01 Sv. Le coefficient Q vaut 1 pour des bêtas, pour des rayons X et pour
des gammas. Q varie de 5 à 20 pour des neutrons selon leur énergie,
et Q est égal à 20 pour des alphas, dont l'énergie
est déposée dans un volume plus petit. Le coefficient N,
lui, est fixé à 0.20 pour les organes reproducteurs, à
0.12 pour la moelle osseuse, le côlon, le poumon, l'estomac, à
0.05 pour la vessie, le sein, le foie, l'œsophage, la thyroïde, et
à 0.01 pour peau et les os. On peut également estimer empiriquement
des coefficients N pour d'autres organismes : les insectes sont 10 à
100 fois plus résistants que les humains aux rayonnements ionisants,
d'où l'idée qu'après une guerre nucléaire généralisée,
il ne restera sur Terre que les blattes et les fourmis.
La complexité des mécanismes conduisant d'une irradiation
à une carcinogenèse rendent la question difficile, et les
études épidémiologiques ne sont pas utilisables. La
relation linéaire sans seuil extrapolée aux faibles doses
implique par exemple qu'il y aura aussi bien 50 cancers supplémentaires
parmi mille personnes recevant 1 Sv, que parmi un million recevant 1 mSv.
Mais ces 50 cancers sont repérables parmi 280, mais pas du tout
parmi 280 000. Malgré de nombreuses réticences, la relation
linéaire sans seuil est utilisée par la plupart des organismes
nationaux et internationaux en application du « principe de précaution
». Depuis 1990, la norme administrative a réduit de
5 à 1 mSv/an le seuil autorisé de dose dépassant la
radioactivité naturelle et médicale (et de 50 à 20
mSv/an pour les professionnels). C'est le millième de la dose qui
augmente de 5% le risque de cancer chez l'adulte.
retour au sommaire |
| Il est peut-être utile de
revenir sur les différentes unités employées au sujet
de la radioactivité : le becquerel correspond à une
transmutation par seconde dans un échantillon, le gray à
un joule d'énergie absorbée par kilogramme d'absorbeur, et
le sievert est égal à un gray pondéré par des
coefficients qui tiennent compte de l'impact de cette énergie
sur tel ou tel organe humain.
On utilise souvent la métaphore des
pommes: si deux enfants se lancent des pommes, les becquerels représentent
le nombre de pommes lancées, les grays l'énergie d'impact
des pommes reçues, et les sieverts différencient les pommes
recueillies dans la main de celles qui frappent les bras, voire l'œil!
Selon les sources (Direction de la protection et de la sécurité nucléaire du CEA, Autorité de Sûreté Nucléaire, Ministère de la Santé, Conseil scientifique des Nations Unies, etc.), les valeurs précises varient quelque peu et donnent des valeurs plus ou moins élevées pour le radon ou pour la radioactivité du sol, plus faibles ou plus importantes pour les applications médicales. Ce n'est pas très surprenant dans la mesure où la radioactivité ambiante varie fortement selon le lieu, selon l'altitude et même selon la météo, et la notion de dose moyenne d'origine médicale n'a pas non plus grand sens: une personne subissant de nombreux examens ou une radiothérapie reçoit bien évidemment une dose de rayonnements très supérieure à celle reçue par une personne ne passant qu'une radiographie dentaire. La principale source d'irradiation naturelle
est le radon, gaz provenant de la transmutation du radium (lui même
descendant de l'uranium) qui se trouve à très faibles doses
dans beaucoup de minéraux du sol, en particulier les granits. Le
radon est un émetteur alpha, il agit donc par contact, lui ou ses
descendants, essentiellement par inhalation, au niveau de la muqueuse des
bronches et des poumons. On estime qu'il est la seconde cause de cancers
du poumon, loin après le tabac.
Les teneurs en radon sont donc très variables, la moyenne en France étant de l'ordre de 30 000 atomes de radon 222 par litre d'air (qui contient 1022 molécules d'oxygène). Cela induit une radioactivité de 63 Bq/m3, conduisant à une dose absorbée de 1.3 mSv par an. Mais ces doses varient beaucoup d'une région à une autre, les régions à sol granitique pouvant la voir doubler ou tripler. Au delà de 400 Bq/m3 dans un logement, il est recommandé d'entreprendre des actions correctrices, essentiellement une meilleure ventilation. Le sol est lui-même naturellement radioactif et contribue en moyenne à hauteur de 0.5 mSv par an à la radioactivité absorbée : cela vient pour 1/3 de l'uranium 238, pour 1/3 du thorium 232 (tous deux émetteurs alpha) et pour 1/3 du potassium 40 (émetteur bêta). La radioactivité du sol est extrêmement variable selon les minéraux qu'il contient : une tonne de sol sédimentaire contient à peu près 3 g d'uranium (et aussi 5 g de potassium 40 et 10 g de thorium), mais une tonne de sol granitique contient 20 g d'uranium. Certaines régions comme le Limousin ou la Corse en France sont de ce fait bien plus radioactives que les plaines du Nord. Il y a des régions aux sols beaucoup plus radioactifs : dans l'état du Kerala, en Inde, la radioactivité naturelle est de 17 mSv/an (avec des pics à 150) et dans la ville de Ramsar en Iran sur les bords de la Caspienne la radioactivité naturelle atteint 260 mSv/an. La radioactivité du sol est, à
l'échelle de la Terre, aussi responsable (pour moitié) de
la chaleur qui y règne en profondeur et qui conduit en particulier
à la liquéfaction des roches du manteau. Cela permet les
mouvements convectifs responsables de la tectonique des plaques. La radioactivité
a donc joué là, indirectement, un rôle essentiel à
l'évolution de la vie sur Terre.
|
Une grande partie des rayons cosmiques est
absorbée par l'atmosphère, mais cela signifie que cet effet
d'écran diminue en montagne, ou en avion, et chaque fois que l'on
va en altitude: la radioactivité due aux rayons cosmiques double
à peu près tous les 1.500 m (0.3 mSv/an au niveau de la mer,
0.6 à 1.500 m, 1.2 à 3.000 m). Un vol Paris-New York communique
à l'équipage et aux passagers une dose de 0.06 mSv (c'était
le double en Concorde qui volait plus haut qu'un Airbus). Le site Internet
http://www.sievert-system.org
permet à chacun de calculer la dose reçue lors d'un vol
quelconque. Si les passagers ne risquent pas grand chose, les équipages
doivent être un peu plus prudents. Habiter en permanence en altitude
augmente sensiblement la dose de rayonnement : si l'on reçoit 0.3
mSv/an à Paris, on en reçoit 1.7 mSv/an à La Paz en
Bolivie (qui se trouve à 3900 m d'altitude). Un simple séjour
d'un mois à 2000 m d'altitude communique une dose de 0.05 mSv (soit
1% d'irradiation supplémentaire).
Notre corps est lui-même radioactif: nous nous irradions nous-mêmes à hauteur de 0.25 mSv/an, essentiellement en raison des aliments que nous avons absorbés et qui nous ont apporté du potassium 40 (présent sur Terre depuis des milliards d'années) et du carbone 14 (cosmogénique lui, et sans cesse renouvelé). Georges Charpak a suggéré que les 0.25 mSv de cette dose annuelle due aux radiations internes (DARI) fourniraient une unité de radioactivité beaucoup plus parlante que les sieverts L'irradiation d'origine médicale est en moyenne de 1.2 mSv/an mais elle varie bien entendu très fortement d'une personne à une autre. De plus cette irradiation est le plus souvent délivrée sur une durée très brève, le débit de dose est donc nettement plus important que lors de l'irradiation continuelle provenant de l'environnement. Pour la plupart des gens, l'imagerie en est la source principale : rayons X des radiographies et des tomodensitographes (scanners), rayons bêtas et gammas de l'iode 131 et gammas du technétium 99 en scintigraphie, gammas d'annihilation des positrons dans la TEP (tomographie d'émission de positrons)
Les doses sont bien entendu beaucoup plus élevées en radiothérapie puisqu'il s'agit là de tuer les cellules (cancéreuses), et des doses de 10 à 100 sieverts sont courantes, mais il s'agit là des doses délivrées dans la tumeur (rappelons que le sievert est une dose par unité de masse).
Ces doses sont fractionnées en plusieurs séances pour faciliter la récupération des cellules saines entre deux séances. 
«Bombe» au cobalt utilisé en radiothérapie © CEA-DPSN Une autre source de rayonnements ionisants, beaucoup plus faible que les précédentes (0.04 mSv/an, soit 1% du total), vient de l'utilisation de sources radioactives dans de multiples secteurs industriels. Certaines d'entre elles sont scellées, c'est-à-dire que le matériau radioactif est isolé dans une enceinte (seuls les rayonnements s'en échappent). En mesurant l'absorption de ces rayonnements, on estime la densité du milieu traversé et on peut contrôler la qualité de l'air, ou la quantité de sédiments dans un fleuve. Des détecteurs de fumée existent sur ce principe. Des jauges radioactives permettent aussi de mesurer l'épaisseur, la densité, ou le niveau d'un fluide dans un réservoir ou une conduite fermées ou peu accessibles.
Des sources radioactives émettrices de rayons gamma (cobalt 60, césium) permettent de stériliser du matériel médical ou des aliments en détruisant les micro-organismes dangereux. On en utilise également dans les musées pour préserver des objets anciens (la momie de Ramsès II a été soumise à ce traitement pour la débarrasser de champignons parasites). D'autres sources radioactives ne sont pas confinées, parce qu'elles servent justement de traceurs : c'est leur déplacement qui est suivi. En marquant un polluant avec un radio-isotope, on peut le suivre son déplacement et en tenir compte pour tracer des routes ou construire des bâtiments. On peut aussi contrôler l'étanchéité de sites de stockage, ou étudier en géologie le déplacement de masses d'air ou de masses d'eau. Les explosions nucléaires, depuis les bombes d'Hiroshima et de Nagasaki jusqu'à la fin des essais aériens, ont contaminé l'atmosphère avec des éléments radioactifs dont certains ont une durée de vie longue comme les 30 ans du césium 137. On mesure nettement la diminution de cette radioactivité depuis l'arrêt des essais atmosphériques, ainsi que le sursaut causé par l'accident de Tchernobyl en 1986. Cette contamination nucléaire représente à peu près 0.02 mSv/an.
Enfin la contribution qui suscite le plus de
réactions, parfois violentes, est celle des centrales nucléaires,
bien qu'à 0.004 mSv/an en moyenne, elle soit de loin la plus faible.
Bien sûr, une moyenne très faible n'interdit pas l'existence
de valeurs localement beaucoup plus élevées, mais on n'a
jamais relevé de hauts niveaux de radioactivité dans l'environnement
des centrales. La principale source de radioactivité vient en fait
des déchets nucléaires, qu'il s'agisse de combustibles devenus
inutilisables ou d'éléments de structure devenus radioactifs.
Cela correspond en France à 1 kg de déchets à faible
et moyenne activité et à 10 grammes de déchets de
forte radioactivité par habitant et par an, bien moins que les déchets
toxiques ou polluants (acides, solvants, métaux lourds, déchets
médicaux par exemple) qui sont aussi plus difficiles à repérer.
Le risque d'un accident nucléaire plane toujours, mais la fusion
du cœur du réacteur de Three Mile Island en 1979 aux USA n'a causé
aucun mort.
retour au sommaire |