| LA DEUXIÈME ETAPE est liée
à la démonstration qu'à chaque dimension biologique
LA
DISTRIBUTION DE DOSE N'EST JAMAIS HOMOGÈNE, et qu'en conséquence,
exprimer les effets par une moyenne est une absurdité a priori.
La démonstration en a été faite dans un tissu au niveau
cellulaire.
Exemple: la distribution de dose d'IODE 131, radionucléide émetteur de rayons gamma et de particules bêta (des électrons), dans une thyroïde cancéreuse avide d'iode. Si on injecte par voie veineuse une dose unique et connue d'iode radioactif 131 et que l'on mesure son incorporation cellule par cellule à l'aide de la microscopie électronique et une sonde de Castaing, on trouve des différences d'incorporation de cellule à cellule de 0 à 100 fois la dose moyenne prévue. Cette constatation est corrélée avec la répartition de la mort programmée des cellules avides d'iode. Le résultat peut s'exprimer ainsi : De deux cellules voisines, irriguées de façon identique, l'une peut ne rien recevoir comme dose, et l'autre être détruite par 100 fois la dose létale théorique! Peu à peu la notion d'inhomogénéité s'est étendue de la cellule aux tissus, et des tissus au corps humain, puis à toute l'espèce humaine: Deux individus recevant la même dose moyenne au même moment n'auront pas la même distribution de dose et donc pas les mêmes effets. En conséquence: il y avait déjà des cellules "à risque" et des tissus "à risque", il y a maintenant des humains "à risque" comme les enfants, les adolescents pour certains radionucléides, les femmes enceintes etc... La deuxième colonne du temple s'est ainsi trouvée sérieusement endommagée! Mais, après un instant de désarroi, les fronts se sont reconstitués: Même si tous les effets sont inégaux et probabilistes, il n'en reste pas moins qu'en général au-dessous du seuil, le fameux mSv par an pour toutes les populations, il n'y avait rien de mesurable pour les uns, des effets à coup sûr pour les autres, il suffit simplement d'oublier que le mSv pour un sujet n'est pas le même que pour son voisin, puisqu'il s'agit d'une moyenne, alors... LA TROISIEME ETAPE: LA BIOLOGIE MOLÉCULAIRE ET LES EFFETS RADIO INDUITS. Notre excellent collègue, Eric SOLARI est venu au Congrès de Paris expliquer la chaîne des effets des rayonnements ionisants pour les molécules (molecular mechanisms of radiation induced cell death, MED. CONFLICT AND SURV. 16, 2000, p. 257) Ce qu'il faut en retenir, au-delà des raffinements biochimiques, c'est que les rayonnements ionisants, X, gamma, ou particulaires, agissent dans la cellule en dehors du noyau. En plus des ruptures de brins de chromosomes qui restent indiscutables, quand ils existent, et qui gardent la possibilité de bénéficier, par les enzymes, d'une réparation parfaite ou fautive, il y a apparition possible d'un signal invisible sur la cellule irradiée. Ce signal va apparaître en cas de division cellulaire, c'est "la mort programmée" ou APOPTOSE. Ce signal peut ne pas être suivi d'effet, cela dépend de certaines protéines de la cellule (celle qui porte le signal est souvent la p52) et de petites formations très actives, les mitochondries, véritables usines chimiques de fabrication en particulier des protéines. (suite)
|
suite:
On connaissait déjà les lésions mesurables du noyau et la production dans le cytoplasme de radiotoxiques appelés radicaux libres, il faut en plus prendre en compte un signal, le plus connu étant celui de l'apoptose. Ces données, en l'état, n'ont pas substantiellement changé les opinions dans les deux camps, jusqu'aux publications de nombreuses équipes de radiobiologistes en Grande-Bretagne, Irlande et aux USA ainsi qu'en France avec les travaux de notre ami CHRISTIAN CHENAL: • A partir de deux séries de faits expérimentaux, ils ont apporté la preuve qu'il y a bien un effet aux très faibles doses, mais pas celui que l'on attendait, c'est ce que nous verrons dans la 2e partie de ce dossier. II - RESPONSABLES MAIS PAS COUPABLES!
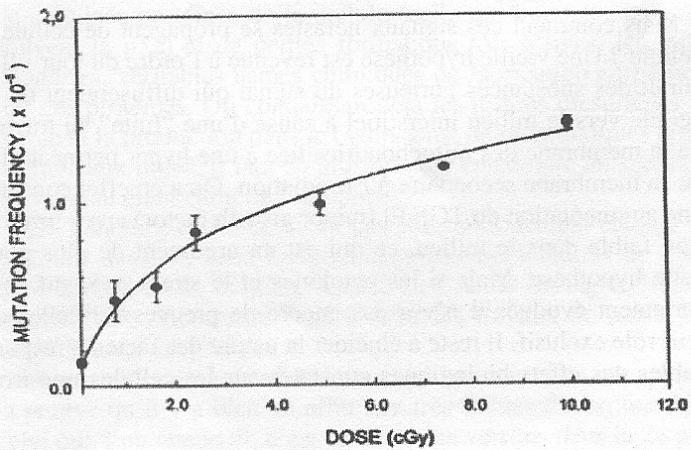
A partir de deux publications, celle, en 1997,
de HEI (1) et celle, en 1999, de WU (2), une nouvelle donne se fait jour
Figure 1 p.16
|